Д.А. Сулегин, И.И. Юрасова
7
Вторая серия опытов была проведена с использованием трех рас-
творов сульфата никеля и NaOH, аналогичных растворам первой
серии, с той лишь разницей, что весь объем щелочи добавлялся в тече-
ние 1 с. Химический состав полученных при этом образцов, рассчитан-
ный по остаточным концентрациям, оказался одинаковым и соот-
ветствовал химической формуле Ni(OH)
1,5
(SO
4
2–
)
0,25
· 4H
2
O. ИК-спектры
этой серии образцов показаны на рис. 6. Как видно, эти спектры подоб-
ны, что указывает на получение гидроксосоли никеля с большим гид-
роксильным числом. Этот же состав подтверждается данными термо-
гравиметрического и калориметрического анализа, приведенными на
рис. 7 и 8, из которых видно, что кривая потери массы имеет три четко
выраженных пика, соответствующих испарению адсорбированной воды
при температуре 70…200 °С, хемосорбированной воды при темпе-
ратуре (350 ± 10) °С и хемосорбированной воды при температуре
430 °С. Серный ангидрид SO
3
десорбируется при температурах более
700 °С [18]. Химическая формула осадков при этом выглядит сле-
дующим образом: Ni(OH)
1,5
(SO
4
2–
)
0,5
· 1,8H
2
O.
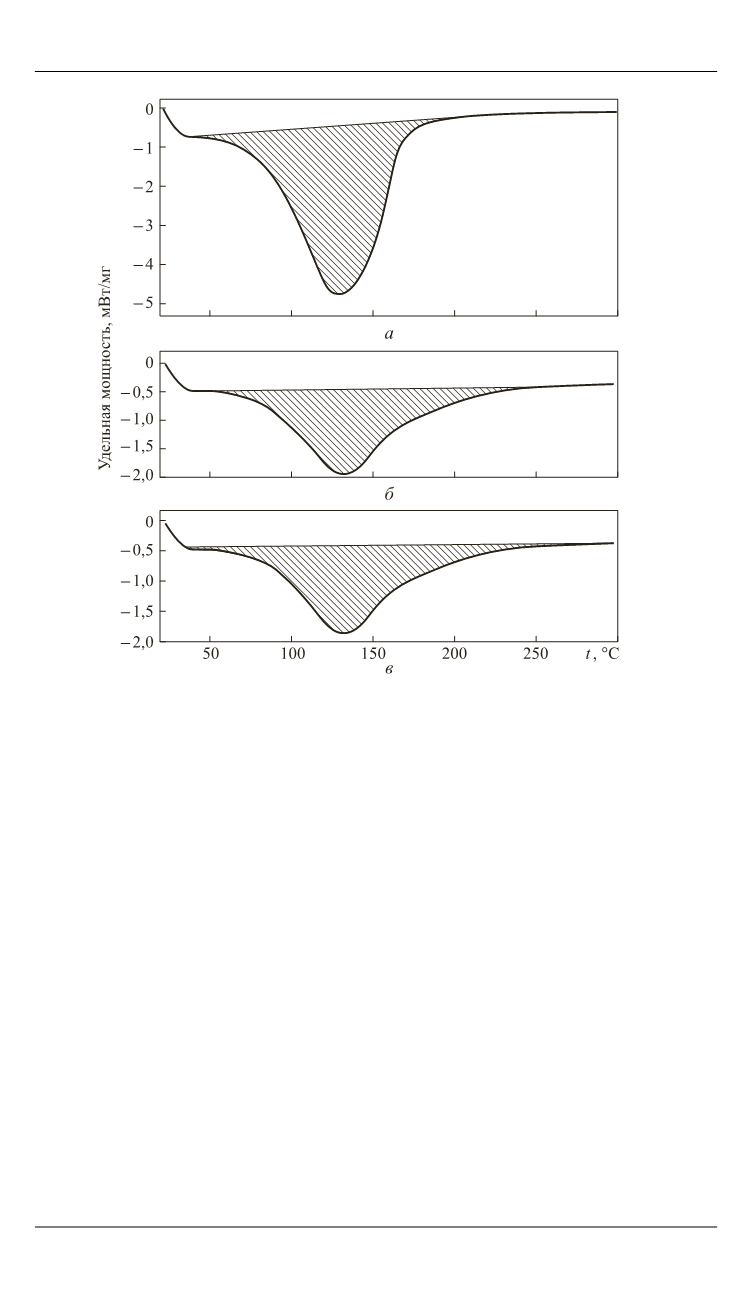
Рис. 5.
Дериватограммы образцов:
а —
1.1;
б —
1.2;
в —
1.3


